18项FDA批准;278个器械获NMPA批准注册文件——医疗器械获批周报(2024.9.13
2024年9月13日至9月19日,动脉橙产业智库重点整理了医疗器械产品国内外获批资讯及数据,涉及18个器械获FDA批准,两个器械获欧盟及其他批准,另有278个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 外科手术产品开发商Alesi Surgical手术烟雾管理设备获FDA批准,并获得新融资
Alesi Surgical因其Ultravision2 IonPencil获得FDA 510(k)许可,该设备在开放手术中切割和凝固软组织,同时管理手术烟雾。该许可扩大了该公司Ultravision2系统的使用范围,该系统已于2023年被批准用于腹腔镜手术。总部位于英国加的夫的Alesi Surgical也获得了500万英镑的新资金,由Mercia Ventures牵头,现有投资者参与,使总资金超过2100万英镑。
2. 可穿戴监测设备研发商OxiWear实时监控设备获得FDA批准
OxiWear的耳戴式氧气监测装置已获得FDA批准,该装置用于连续、实时测量血氧饱和度和脉搏率。该设备提供了无与伦比的准确性和便利性,为患者和医疗保健提供者提供了对重要血氧饱和度数据的持续访问。它的连续数据收集能力对于早期低氧血症检测至关重要,可提供救生警报。
3. 安斯泰来无创数字健康解决方案获FDA批准,用于心力衰竭管理
Astellas Pharma Inc.宣布,用于心力衰竭管理的非侵入性数字解决方案DIGITIVA™已被FDA列为I类医疗器械软件(SaMD),并免于510(k)上市前提交。DIGITIVA是Astellas在美国推出的首个数字健康服务,旨在与心力衰竭患者的护理团队合作,使他们能够积极管理自己的健康。它包括一个数字听诊器,一个具有教育内容的智能手机应用程序,以及一个临床审查小组,该小组负责监测患者数据并通知医生干预需求,旨在改善临床结果。
4. 马斯克盯上了盲人,Neuralink下一代脑机接口产品获FDA批准
马斯克旗下Neuralink的大脑植入芯片Blindsight获FDA“突破性设备认定”,有望让盲人重获光明。该设备通过植入大脑直接刺激视觉皮层,使盲人产生光感并形成影像图形,已初步证明临床效果显著改善。Blindsight设定了低分辨率和高分辨率两个阶段目标,获认证后将优先审查,缩短审批时间。
5. 全球首个,百多力用于左束支起搏LBBAP导管获FDA批准
百多力公司的Solia S导联和Selectra 3D导管获得FDA批准,可用于左束支起搏(LBBAP),该疗法是治疗心力衰竭的新替代方案。FDA的批准基于临床试验数据,显示95.7%的患者成功植入LBBAP,且并发症率低。
6. 无需手术不含药,可消化设备开发商Epitomee减肥胶囊获FDA批准上市
Epitomee Medical宣布其减肥胶囊Epitomee减肥胶囊获FDA批准上市。Epitomee减肥胶囊是一种可以口服的减肥医疗器械,旨在为BMI指数为25-40 kg/m²的成年人提供体重管理,同时进行饮食和锻炼。Epitomee减肥胶囊由生物相容性赋形剂、食品添加剂和食品接触材料制成。在遇水且一定PH值下,Epitomee减肥胶囊将自动膨胀成一个灵活的三角形水凝胶(每边长约6.2cm、宽约12mm)。三角形水凝胶在水溶液中将缓慢降解。
7. 医疗设备开发商Obvius Robotics的CERTA Access系统获FDA批准
Obvius Robotics的中心静脉导管插入术(CVC)CERTA接入系统已获得FDA突破性设备指定。CERTA访问系统旨在改善重症监护环境中的患者护理和血管访问程序。CVC手术每年在全球范围内进行超过2000万次,并发症发生率(4%-11%)各不相同,突出表明需要更好和更一致的结果。FDA的计划旨在通过更快的开发、评估和审查,加快患者获得此类医疗设备的速度。
8. 美国食品药品监督管理局批准Neuroblade系统用于微创神经外科
Clearmind Biomedical的Neuroblade系统已获得FDA 510(k)的许可,Neuroblade系统是一种神经内窥镜检查系统,可实现具有可视化、照明、冲洗、抽吸、凝血和动力清创等功能的微创手术。该系统包括Neuroblade、Europad和Clearpath组件,旨在简化神经外科手术并改善患者预后。
9. 创新诊断产品研发商T2 Biosystems旗下5种真菌核酸检测试剂盒获FDA批准上市
T2 Biosystems的血液检测试剂盒获FDA批准,可快速检测五种常见念珠菌,有望改善儿童败血症诊疗,缩短住院时间并减少费用。
10. 医疗设备开发商Piccolo Medical导管引导技术获FDA批准
Piccolo Medical已获得FDA批准,其PM2系统采用ECGuide(一种新的导管引导技术)。ECGuide使用ECG实时确定导管尖端位置,提供胸部X射线替代方案。Piccolo首席执行官指出,盲目插入会带来风险和成本,ECGuide旨在消除广泛采用的障碍。这扩大了Piccolo的产品线,旨在减少每年影响800多万患者的中心静脉导管插入并发症。由私人投资者和美国国立卫生研究院拨款资助的Piccolo此前已获得SmartPICC系统的许可。
11. Shockwave用于PAD、CLTI的新型IVL导管获得FDA批准
Shockwave Medical推出新型IVL导管E8,获FDA批准,用于治疗钙化股腘动脉和膝下外周动脉疾病,包括复杂慢性肢体威胁性缺血。
12. 医疗设备初创公司Forest Devices旗下脑电图分析产品获FDA批准上市
成立于2015年的匹兹堡初创公司Forest Devices近日宣布,其信号模型RE系统已获得FDA 510(k)许可,这是该公司首次获得FDA许可。该系统利用脑电图技术和新型快速部署的耳机和便携式设备,在5-7分钟内分析患者的神经系统状态,提供关键的见解。Forest Devices旨在为面临急性神经系统问题的患者提供及时、客观、实时的信息。
13. GE医疗新型脑成像工具获FDA批准,治疗阿尔茨海默病
GE HealthCare宣布,FDA已批准其新的成像工具MIMneuro和百分位数缩放软件,用于评估潜在的阿尔茨海默氏病。该工具获取PET淀粉样蛋白图像,自动生成定量结果,并将数据显示在标准化报告中。FDA 510(k)清除率涵盖了对基于PET的淀粉样蛋白成像分析和定量进行百分位数缩放。这种新工具可以帮助临床医生更自信地确定患者大脑中淀粉样斑块的密度,这是阿尔茨海默病评估的一个关键方面。该公司希望通过这项创新扩大患者获得个性化护理的机会。
14. 血糖监测服务提供商Senseonics宣布365天全天候检测血糖CGM获FDA批准上市
Senseonics的下一代Eversense 365 CGM系统已获得FDA批准,成为世界上第一台365天连续血糖监测仪。该系统专为18岁及以上的1型和2型糖尿病患者设计,也可以作为集成的CGM系统与兼容的医疗设备一起工作,例如自动胰岛素输送系统中的胰岛素泵。
15. 飞利浦增强型LumiGuide血管内导航导丝获FDA批准
飞利浦已宣布FDA批准其增强型160cm LumiGuide血管内导航导线,该导线采用该公司突破性的光纤RealShape(FORS)技术。这项技术首次由教授和血管外科医生Carlos Timaran在复杂的主动脉瘤修复过程中用于患者,标志着自2020年临床推出以来,第1000名患者接受了FORS治疗。更长的电线使美国临床医生能够看到更广泛的导管,从而将该技术的使用范围扩大到美国的更多患者。
16. 强生全新冲击波球囊Shockwave E8获FDA批准上市
强生推出新款冲击波球囊Shockwave E8,获FDA批准,可优化钙化股腘动脉和膝下外周动脉疾病治疗,包括慢性肢体威胁性缺血,其80mm长球囊和8个发生器可治疗更长病变。
17. Withings Sleep Rx垫获得美国食品药品监督管理局510(k)批准
Withings是一家关联健康技术公司,其Sleep Rx Mat(一种专为在家诊断睡眠呼吸暂停而设计的设备)已获得FDA 510(k)许可。该垫具有一个气动传感器,可测量呼吸频率、身体运动和连续心率,同时还可跟踪睡眠周期和干扰。Withings Health Solutions副总裁Antoine Robiliard对将Sleep Rx推向美国市场表示兴奋,并表示它为睡眠呼吸暂停的诊断和管理创造了新的范例。在其他新闻中,Withings推出了U-Scan,一种使用尿液分析的生物标志物评估平台,并与Medable合作,使用其连接的设备进行远程监测,进行分散的临床试验。
18. 血管介入医疗技术开发商Biotronik起搏导线和输送导管系统获得FDA批准
Biotronik宣布,其用于左束支区域起搏(LBBAP)的Selectra 3D导管和Solia S导线已获得FDA批准,使其成为FDA批准的第一个也是唯一一个针驱动导线和专用输送导管系统。该产品已在全球8万多名患者中使用,支持不断发展的心脏自然传导系统起搏技术。BIO-CONDUCT试验的结果显示出良好的结果,导线和导管的组合证明非常可靠。2024年HRS提供的数据显示植入成功率高,铅相关并发症低。Biotronik致力于为医生提供创新产品和解决方案,以促进护理。
二、欧盟及其它
1. Venus Concept宣布澳大利亚监管机构批准Venus Bliss MAX
Venus Bliss MAX为身体治疗需求提供了全面的解决方案,采用了该公司三项市场领先的技术:(MP)2用于减少脂肪团和皮肤治疗的敷贴器,FlexMax EMS用于肌肉调理的敷贴器,以及用于减肥的二极管激光。Venus Concept总裁兼首席运营官Hemanth Varghese博士对将该设备引入澳大利亚市场表示兴奋,相信它将复制其全球成功。
2. 第二款,爱德华生命科学经导管瓣膜修复系统获批
爱德华生命科学的Pascal Precision经导管瓣膜修复系统获加拿大卫生部批准,用于治疗症状性二尖瓣反流,该系统已获FDA和CE认证,可治疗二尖瓣和三尖瓣反流,具有独特的设计和技术优势。
国内获批
NMPA最新获批器械产品明细
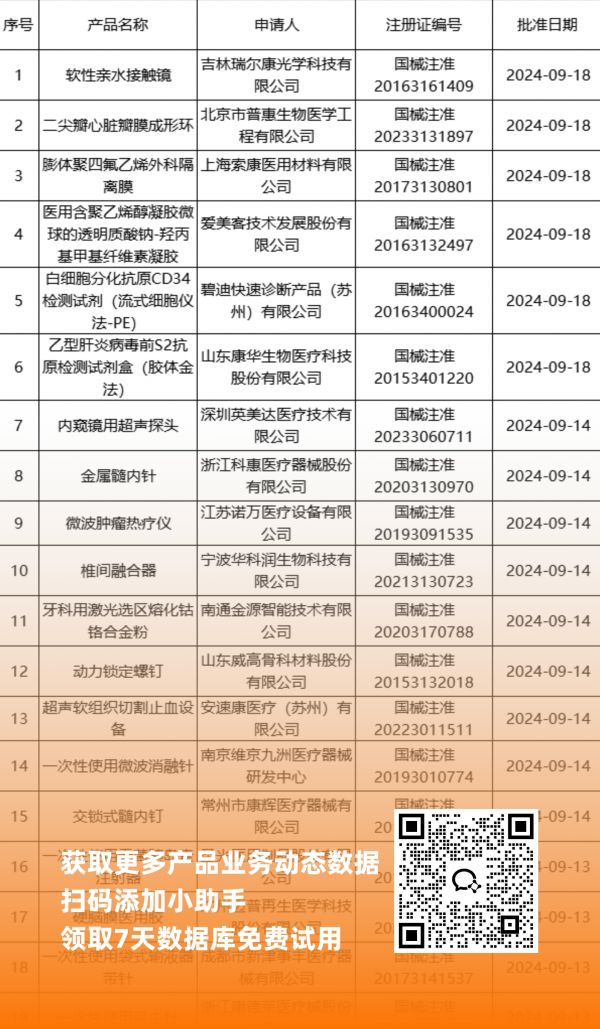
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉橙仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。
国科恒泰与动脉网携手打造爱经销模式推广会暨渠道交流会,满足医疗器械生产企业与经销商之间对接需求,同步在成都、太原、杭州、西安等地举办线下专场,点击图片立刻对接↓

相关知识
FDA批准首款新型减肥器械
FDA 批准肥胖治疗器械 AspireAssist
继NMPA创新医疗器械特别审批后 康博刀®再获美国FDA“突破性设备认定”
692款FDA批准的人工智能医疗器械:放射科领跑应用大潮!
如何获得FDA注册批准食品,饮料和膳食补充剂
我国已批准156个创新医疗器械
【健康·生活】277个创新医疗器械获批上市
FDA近三年批准的121款数字医疗产品盘点
创新医疗器械获批上市,肿瘤治疗设备市场潜力巨大
华为OPPO歌尔在列,2020这些可穿戴设备已过医疗器械认证
网址: 18项FDA批准;278个器械获NMPA批准注册文件——医疗器械获批周报(2024.9.13 https://www.trfsz.com/newsview649339.html
推荐资讯
- 1发朋友圈对老公彻底失望的心情 12775
- 2BMI体重指数计算公式是什么 11235
- 3补肾吃什么 补肾最佳食物推荐 11199
- 4性生活姿势有哪些 盘点夫妻性 10428
- 5BMI正常值范围一般是多少? 10137
- 6在线基础代谢率(BMR)计算 9652
- 7一边做饭一边躁狂怎么办 9138
- 8从出汗看健康 出汗透露你的健 9063
- 9早上怎么喝水最健康? 8613
- 10五大原因危害女性健康 如何保 7828